Para um bom entendimento e aplicação da volumetria de oxidação-redução é necessário que se tenha solidificado os conceitos da eletroquímica também.
Dentro desse contexto podemos apontar um fato bastante corriqueiro em nosso dia a dia, que é a corrosão de metais. As reações de corrosão acontecem, de maneira espontânea, quando um metal é atacado por alguma substância e convertido em um composto não desejado. Um bom exemplo é a ferrugem, que nada mais é que a corrosão do ferro.
A ferrugem requer tanto oxigênio quanto água, e o processo pode ser acelerado por outros fatores, como: pH, presença de sais e desgaste do ferro (BROWN et al., 2016).
Com base nos estudos da eletroquímica, responda as seguintes questões:
a) Tendo as duas semirreações que mostram o processo espontâneo de ferrugem (corrosão do ferro), indique qual delas ocorre no cátodo e qual ocorre no ânodo: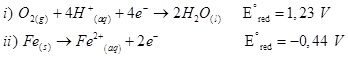
b) Para proteger o ferro do processo corrosivo, é possível fazer um revestimento com outro metal. Dessa forma, evita-se que a água e o oxigênio atinjam a superfície do ferro. Para essa finalidade é necessário que o metal de revestimento seja mais fácil de oxidar que o ferro. Com base na Tabela 1, de valores de potenciais padrão de redução, qual metal (ou metais) você escolheria para essa finalidade (revestimento)? Justifique sua resposta.
Envie sua primeira dúvida gratuitamente aqui no Tira-dúvidas Profes. Nossos professores particulares estão aqui para te ajudar.
Envie sua primeira dúvida gratuitamente aqui no Tira-dúvidas Profes. Nossos professores particulares estão aqui para te ajudar.
a) Em uma célula eletroquímica, o cátodo é o eletrodo em que ocorre a reação de redução, ou seja, ocorre o ganho de elétrons, enquanto que o ânodo é o eletrodo em que ocorre a reação de oxidação, ou seja, ocorre a perda de elétrons. Dessa maneira, podemos observar que a semirreação i) o oxigênio sofre redução, passando do estado de oxidação -1 (O2) para -2 (H2O), já a semirreação ii) o ferro sofre oxidação, passando do estado de oxidação 0 (Fe) para +2 (Fe2+).
b) Para proteger o ferro, é necessário utilizar um metal que possua potencial de oxidação maior que o ferro (este será o metal de sacrifício, pois irá oxidar no lugar do ferro), em se tratando de potencial de redução, o contrário é verdadeiro, ou seja, o metal deve possuir potencial de redução menor que o do ferro e, assim, este metal de sacrifício sofrerá oxidação primeiro. Como pode-se observar na tabela, os metais que possuem os potenciais de redução menor que o Fe são o Zn e o Al.
Envie sua primeira dúvida gratuitamente aqui no Tira-dúvidas Profes. Nossos professores particulares estão aqui para te ajudar.